サプリ制度再設計の核心問う(前) 米欧ASEAN比較で見える制度の前提
厚生労働省と消費者庁でサプリメント規制の見直し議論が進む中、ウェルネスデイリーニュース編集部は㈱グローバルニュートリショングループ(GNG、東京都豊島区)の代表取締役・武田猛氏に取材した。米国、EU、ASEANの制度を比較すると、サプリメントの定義や安全性の捉え方には根本的な違いが存在する一方、日本では制度上「サプリメント」が定義されていないという構造的課題が浮かび上がる。武田氏は「サプリメンティッドフード(Supplemented Food)」という新たな概念を提示し、従来の枠組みを超えた制度設計の必要性を指摘した。
「サプリメントを巡る国際的な制度の歴史を紐解くと、単なる名称の違いを超えた、各地域の食品安全思想の深い差異が浮かび上がってくる」という同氏に、新たなサプリメント規制の在り方について聞いた。
サプリ規制見直し議論が本格化
厚生労働省と消費者庁において、サプリメントの規制の在り方に関する議論が本格化している。消費者庁で、サプリメントの「定義」と「製造管理(GMP)の在り方」について、事業者・消費者の計10団体からヒアリングが行われた。その中で、米国と欧州におけるサプリメント規制の在り方が紹介された。しかし、米国・DSHEA(ダイエタリーサプリメント健康教育法)が成立したのは1994年のこと。また、EU健康・栄養表示法は2007年(補足説明:EUでは、サプリメント自体は02年のFood Supplements Directive(フードサプリメント指令)で整理され、その後、07年の健康・栄養表示規則で表示面(ヘルスクレームなど)が補強されました)と20年近く前のことになる。
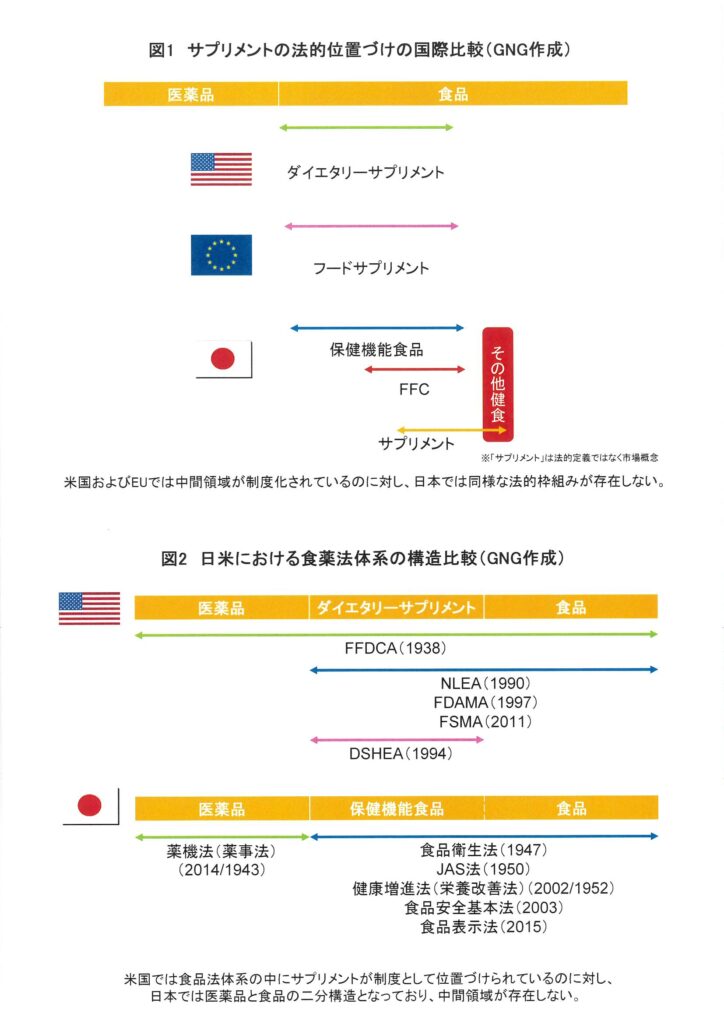
アメリカの「ダイエタリーサプリメント(Dietary Supplement)」は、文字どおり「食事を補うもの」という位置付けだ。1990年に制定された栄養表示教育法を土台として、94年にDSHEA(ダイエタリーサプリメント健康教育法)が成立した。さらに見落とされがちな重要な転換点として、2011年に施行されたFSMA(米国食品安全強化法)がある。この法律は、食品全体の安全管理の枠組みを大きく見直し、サプリメントを含むすべての食品について、従来の適正製造基準(cGMP)に加え、予防的管理の考え方を統合した管理体制を導入した。サプリメントについては、それ以前からPart 111に基づくGMP規範が存在していたが、FSMAの導入により、食品全体としての管理体系との整合性が一層強化された形である。
このような制度の展開を踏まえると、製品の剤型や個別の原材料の区分のみに着目した議論は、本質的な論点とは言い難い。米国では、製品の形態にとどまらず、原材料の調達から製造、流通に至るまで、サプライチェーン全体を視野に入れた管理責任の考え方が強まっている。
EUの「フードサプリメント(Food Supplement)」は、食品の一部としての位置付けが明確で、その規制思想は徹底した「源流管理」にある。ノベルフード制度とポジティブリスト制度を組み合わせることで、承認されていない成分は食品にもサプリメントにも使用できない仕組みを構築している(1997年5月以前にEU域内で食経験があるものは除く)。この厳格さはイノベーションを阻害するという批判も現地コンサルタントの一部から上がっているが、安全性の担保という観点では極めて高い水準を実現している。
各国で異なる定義と制度思想
ここで前提として確認しておくべきは、各国におけるサプリメントの定義そのものが大きく異なる点である。武田社長は具体的に次のように説明する。
米国のダイエタリーサプリメントは「ビタミン、ミネラル、ハーブまたはその他植物、アミノ酸などの食用成分やその濃縮物、抽出物などを摂取するために加工された製品であり、一般的な食品や食事そのものではない」と明確に区別されている。すなわち、通常の食事とは異なる目的で設計された食品であるという位置付けが制度上明確に与えられている。
EUにおいても同様に、フードサプリメントは「通常の食事を補足する目的で、栄養学的または生理学的効果のある成分を濃縮した形で含有する製品」と定義されている。さらに、その形態もカプセル、錠剤、粉末パック、液体など、少量摂取が可能な形であることが要件とされている。ここでも、通常食品とは異なる目的と設計が制度上明示されているのである。
ASEANのヘルスサプリメントはさらに踏み込んでいる。武田氏によれば、「食事を補完し、ヒトの健康的な身体機能を維持、強化または向上させることを目的とした製品」と定義されており、その対象成分にはビタミンやミネラルだけでなく、アミノ酸・脂肪酸・酵素・プロバイオティクス・天然由来抽出物、さらには安全性が証明された合成成分まで含まれるとされる 。この定義は、単なる栄養補給にとどまらず、健康機能の維持・強化という目的を明確に含んでいる点に特徴がある。
このように、米国、EU、ASEANはいずれも、サプリメントという対象を制度上明確に定義している。これに対し、日本では事情が大きく異なる。保健機能食品制度は存在するものの、それは表示や機能に関する制度であり、「サプリメントとは何か」という定義を与えるものではない。
「日本においてサプリメントは制度上存在していない」という武田氏の指摘は、制度理解の出発点として極めて重要である。
こうした定義の違いは、そのまま制度思想の違いにつながる。武田氏は、日本を「分業+事後確認型」、米国を「設計責任型」、EUを「ルール拘束型」と区別している。
日本は問題が起きていないかを確認する構造であり、米国は問題が起きないように製品を設計する責任を企業に課し、EUは問題が起きうる製品を制度的に市場に入れない構造を採用しているという。
この違いは、安全の捉え方にも表れている。日本では「問題が起きていない状態」が安全とされるのに対し、米国では「問題が起きないよう設計された状態」、EUでは「問題が起きうるものは排除された状態」が安全とされる。すなわち、日本は結果の確認、米国は設計段階での担保、EUは制度による予防という構造である。

そして最も新しい制度モデルとして注目すべきが、ASEANの「ヘルスサプリメント(Health Supplement)」だという。2015年以前に原案が策定されたこの制度では、食事の補完という従来の機能に加えて、「人の健康的な身体機能の維持・強化・向上を目的とした製品」という定義が盛り込まれている。アメリカ、EUの制度をそれぞれ10年の間隔で参照しながら、時代の変化に対応した定義を採用したこのモデルは、現時点で最も時代にマッチした制度設計と評価できる。
今回の消費者庁の検討会では、アメリカとEUの制度のみが参照されており、ASEANモデルが議論の俎上に載っていないことは、制度設計の視野の狭さを示していると、武田社長は指摘する。
<武田 猛 氏 プロフィール>
麻布大学環境保健学部卒業、法政大学大学院経営学専攻修士課程修了。
アピ㈱、サニーヘルス㈱を経て2004年1月、㈱グローバルニュートリショングループ設立、現在に至る。国内企業の新規事業の立ち上げ、新商品開発、マーケティング戦略立案などのコンサルティングや海外市場進出の支援、海外企業の日本市場参入の支援を行う。現在まで、国内外合わせて800以上のプロジェクトを実施。
経 歴:1986年 麻布大学 環境保健学部卒業、1986年 アピ株式会社入社、1997年 法政大学大学院 社会科学研究科経営学専攻修士課程修了(MBA)、1998年 サニーヘルス株式会社入社、2004年 (株)グローバルニュートリショングループ設立後、現在に至る。
著 書:「健康食品ビジネス大全」(パブラボ社、2011年10月)、「健康食品ビジネス大事典」(パブラボ社、2015年8月)、共著「ヒットを育てる!食品の機能性マーケティング」(日経BP社、2017年4月10日)
活 動:2014年度、消費者庁委託事業として栄養表示義務化および機能性表示創設に伴う消費者教育に関するワーキンググループ委員。同16~18年度にかけ、農林水産省委補助事業「第6次産業化促進技術対策事業」および「食産業における機能性農産物活用促進事業」の検討委員会委員長を歴任。
2018年 機能性表示食品届出指導員養成講座 講師、2019年~21年 機能性表示食品普及推進協議会 会長、一般社団法人通販エキスパート協会 認定スペシャリスト、機能性表示食品届出アドバイザー養成講座 認定講師。
(つづく)
【田代 宏】





















