17年通知改正へ、厚労省が改正案 指定成分GMPとの整合図る
錠剤やカプセル剤などの健康食品(サプリメント)の安全性確保に関する考え方を示す通称「17年通知」が改正される。適正製造規範(GMP)に基づく製造を義務付けている指定成分等含有食品の製造・加工基準告示や留意事項の内容にかなり寄せた改正が行われる。原材料の安全性に関する科学的評価、その上での適正な製品設計、そしてGMPに基づく製造・品質管理や原材料の安全性確保といった取り組みを「自主的」に進めることが、事業者に求められる。機能性表示食品などの保健機能食品を含む、錠剤やカプセル剤などの健康食品全般が対象となる。
パブコメ実施へ、今年度内に改正目指す
所管する厚生労働省では、改正案を取りまとめた後、パブリックコメントを行った上で、17年通知を改正する考え。サプリメントの製造・品質管理に詳しい業界関係者からは、「どこまでいっても求められるのは『自主的な取り組み』だが、要求されるGMPのレベルが高まる」とする見方が上がる。
厚労省は30日、17年通知の改正案を公表した。17年通知は、厚労省が平成17年(2005年)に通知したもので、「錠剤、カプセル状等食品の適正な製造に係る基本的な考え方について」と「錠剤、カプセル状等食品の原材料に安全性に関する自主点検ガイドライン」の2大要素で構成。厚労省はこれを通じて、安全性確保に必要となる、個々の製品品質の均質化を図るため、自主的にGMPに取り組むよう健康食品業界と事業者に求めてきた。
17年通知の改正案は、同日開催された、厚労省の諮問機関「薬事・食品衛生審議会」のうち食品衛生分科会新開発食品調査部会(曽根博仁部会長=新潟大学大学院教授)の俎上に載った。通知改正を担当する厚労省食品基準審査課新開発食品保健対策室は、改正の目的について、かい離が生じていた平成17年通知の内容と、指定成分等含有食品に義務付けているGMPとの整合を図ること、従来の「考え方」ではなく「ガイドライン(指針)」として提示し通知の位置づけを明確にすること、全ての関係事業者にGMPの考え方を浸透させること、全ての関係事業者が原材料の科学的安全性を適切に評価できるようにすること──を挙げた。
17年通知を改正するために、厚生労働科学研究「健康食品の安全性確保に資する情報提供、品質確保、被害情報収集体制の構築に関する研究」(2018~2020年)などを通じた検討を行ってきたという。
「考え方」ではなく「ガイドライン(指針)」
改正案によれば、新たな17年通知は、「錠剤、カプセル剤等食品の原材料の安全性に関する自主点検及び製品設計に関する指針(ガイドライン)」と「錠剤、カプセル剤等食品の製造管理及び品質管理(GMP)に関する指針(ガイドライン)」の2要素で構成される。GMP指針には、これまで考慮されていなかった「バリデーション」の実施が新たに盛り込まれる。バリデーションについて改正案では、「製品の製造等を行う施設の構造設備、手順、工程その他の製造等に係る管理及び品質管理の方法が、期待される結果を与えることを検証し、これを文書とすること」と定義する。要は、あらかじめ定めた規格と品質の合致した製品が途切れなく製造されることを担保し、それを文書化する、ということ。
現行17年通知の別紙で示している「GMPを実施した製造工程管理の関係図」も見直される。改正案では以下の図(厚労省公表資料をキャプチャ)を示している。GMPとは概念の異なる衛生管理については、欄外に「食品衛生法に基づく衛生管理も実施すること」と示すにとどまっている。HACCPに基づく衛生管理の実施を求めているかたちだが、業界関係者からは、「GMPとHACCPをどう共存させるかが課題」だとする声が聞かれる。30日の新開発食品調査部会での審議でも委員から、「この図の中にHACCPのことも加えるべきではないか」とする意見が上がった。
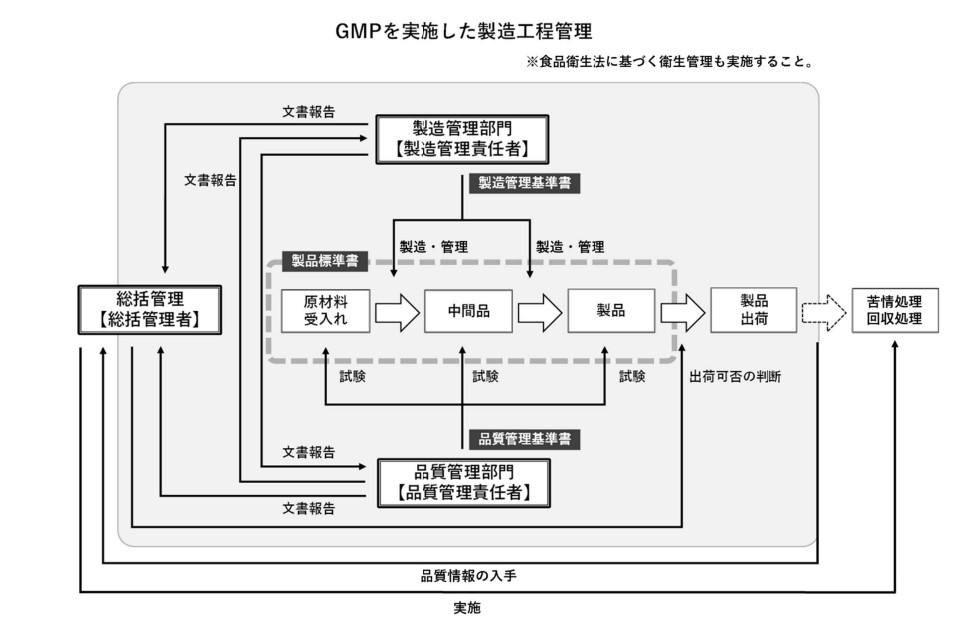
この日の審議では、他にも意見が上がった。新開発食品保健対策室では、意見を踏まえて改正案を修正した上で、パブリックコメントを行う。そして食品衛生基準行政が消費者庁に移管される前、今年度内の改正を目指す。
【石川太郎】
関連資料(厚労省ホームページへ)
:「錠剤、カプセル状等食品の適正な製造に係る基本的考え方について」及び「錠剤、カプセル状等食品の原材料の安全性に関する自主点検ガイドライン」の改正案
:改正の経緯・現状、課題・今後の方針(案)、今後の予定
関連記事
:17年通知改正ある?【厚労省に聞く】 健康被害未然防止と製造品質管理の関係
:健康食品リスク管理、現状改善に本気 厚労省、健康被害情報の収集体制を強化






















