国内製造サプリメントに有害事象 【小林製薬の紅麹問題】問われる安全性と品質の確保
小林製薬㈱(大阪市中央区、小林章浩社長)が販売する機能性表示食品のサプリメントを使用した複数の消費者に有害事象が生じた問題は、安全性や品質の確保の観点から健康食品業界に重大な影響を与えそうだ。機能性表示食品の品質をめぐっては、機能性関与成分の含有量が表示値を下回る製品が消費者庁の買上調査で見つかり、公表されたばかりだった。
機能性表示食品は国が定めた制度に基づく「保健機能食品」の1つ。その使用によって生じた有害事象は、制度を所管する消費者庁や、食品安全監視・指導行政を担当する厚生労働省など国の対応も問われることになりそうだ。国民の3人に1人が使用していると言われ、1兆円超とされる市場規模がありながら、法律上の定義が存在しない健康食品・サプリメントをめぐり、産業界や行政の緊張感が一気に高まっている。
1月中旬に最初の報告、小林社長「判断が遅かった」
22日夕、小林製薬は大阪の本社内で緊急会見を開き、同社で販売する機能性表示食品のサプリメント『紅麹コレステヘルプ』を摂取した複数の消費者に、腎疾患の有害事象が生じたことを明らかにした。同製品と有害事象の因果関係は確定されていないものの、22日夕時点の有害事象報告件数は40~70代の男女13人に上るという。
うち6人が入院(5人はすでに退院)し、7人が通院。入院患者の中には一時、透析が必要になった人が2人いた。同製品は2021年2月に発売。今年2月末までに約110万袋を販売したという。有害事象の公表を受けて、消費者からの被害報告が増えていく可能性がある。
2時間近くに及んだ会見には小林社長をはじめとする同社役員ら4人が出席。同製品の使用を直ちに中止するよう購入者らに求めた。それを呼び掛けるために緊急で会見を開いたという。
ただ、同社が有害事象の報告を最初に医師から受けたのは今年1月中旬で、今月15日までに報告件数が13人に達していた。公表までの間、原因究明に当たっていたなどと同社は説明しているが、対応の遅れを指摘する声も上がる。
会見で小林社長は、「2月初旬の段階で回収の覚悟をもった」とした上で、「事実確認、原因究明にかなり努力したが、結果として時間が掛かってしまい大変申し訳なく思う。判断が遅かったと言われれば、そのとおりだと感じる」と釈明した。
消費者庁が策定した機能性表示食品の届出ガイドラインには、健康被害情報を事業者(届出者)が入手した際の対応指針が明記されている。「評価の結果、届出食品による健康被害の発生及び拡大のおそれがある場合は、消費者庁食品表示企画課へ速やかに報告する」とあるが、小林製薬が報告したのは記者会見の前日。「自主回収すると伝えられたが、会見ほどに詳細な説明はなかった」と同課は22日夜、取材に話した。
原材料供給も 影響の広がり必至
小林は会見で自主回収も発表。対象製品は、有害事象が生じた『紅麹コレステヘルプ』の他に、同製品と同じ原材料(紅麹)を配合したサプリメント『ナイシヘルプ+コレステロール』、『ナットウキナーゼ さらさら粒GOLD』の3製品で、いずれも機能性表示食品。各製品の販売チャネルには通信販売もあるが、ドラッグストアなど店頭販売の割合が多かった。回収製品数は30万袋に上る。
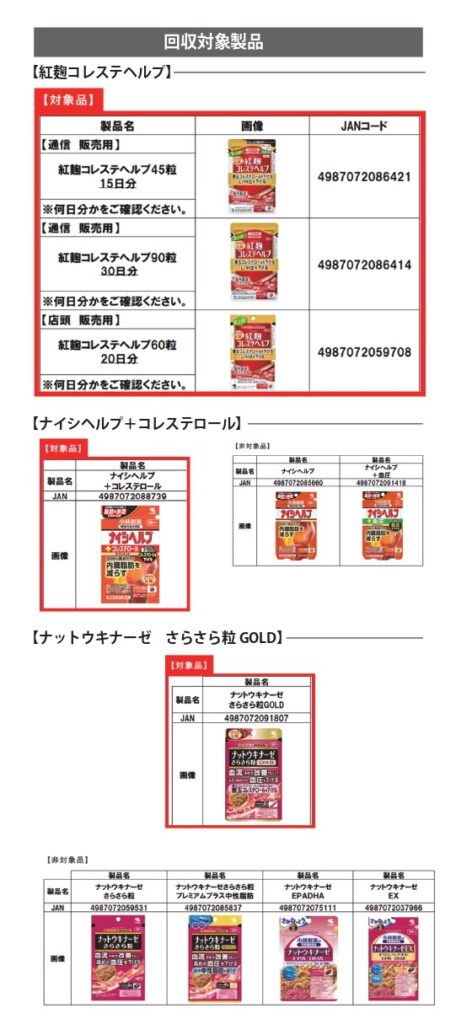
『ナイシヘルプ~』、『ナットウキナーゼ~』は地域を限定したテスト販売にとどめていたと言い、それぞれ販売数量は100~200袋と少ない。ただ、各製品に配合していた紅麹は同社の自社製造品。グループ会社を通じて外部の企業にも販売していたため、影響の広がりは避けられない。不可解なことに同社は今月、グループ会社から供給される同社の紅麹を配合した機能性表示食品が他社から発売される旨を伝えるニュースリリースを発表。外部企業への紅麹原材料の販売を推進していきたい考えを示していた。
同社が紅麹の原材料販売や機能性研究などに着手したのは2016年。メディカル事業も手がけるグンゼ㈱(大阪市北区)から事業譲渡を受けてのことだった。小林製薬によると、今回の有害事象発生を受けた自主回収費用の総額は概算でおよそ18億円に上る見通し。別途、有害事象が生じた消費者への補償費用などが生じる可能性もある。
有害事象が生じた原因は今のところ定かではない。ただ、同社の説明によれば、機能性関与成分の米紅麹ポリケチドを含む、同社の大阪工場(昨年末までに閉鎖)で製造した原材料の紅麹に、腎疾患症状を引き起こす物質が含まれていた可能性が今のところ濃厚だ。原因が特定されるまで、国内の受託製造企業に委託していた最終製品製造時に混入した可能性を拭い去ることはできないが、「原材料の品質に対する要求が厳しい」(業界関係者)同社としての原材料の安全性評価、製造管理、品質保証のあり方が問われることになる。
厚生労働省も対応に動いている。食品基準審査課は22日夜、取材に対して「管轄の自治体で調査中」と答えた。
厚労省は今月、健康食品の安全性を確保するための新たなガイドラインとして、「いわゆる『健康食品』・無承認無許可医薬品健康被害防止対応要領」(新・平成14年通知)と「『錠剤、カプセル剤等食品の原材料の安全性に関する自主点検及び製品設計に関する指針(ガイドライン)』及び『錠剤、カプセル剤等食品の製造管理及び品質管理(GMP)に関する指針(ガイドライン)』」(新・平成17年)を発出しており、さっそく両通知の実効力が問われる。
原材料の安全性に関する自主点検などを健康食品関連事業者に求める新・平成17年通知は4月以降、消費者庁が所管する。また、健康被害報告の届出などを事業者に義務付ける指定成分等含有食品の指定に同庁も関与することになっており、今後の同庁の対応が注目される。
小林製薬と編集部の一問一答を紹介するとともに、原因について考察したい。(⇒つづきは会員専用ページへ)
【石川太郎】
関連記事:小林製薬「紅麹製品」自主回収に思う 【緊急寄稿】東京大学名誉教授 唐木英明
:小林製薬の紅麹問題、宝酒造にも影響 日本酒10万本を自主回収
:小林製薬の紅麹、配合食品が他社から ZERO PLUSが機能性表示食品のおせんべい
:消費者庁、品質管理の徹底求める 機能性表示食品買上調査、成分含量下回る製品発覚受け
(冒頭の写真:会見する小林製薬の小林章浩社長。毎日放送ライブより/文中の画像:小林製薬の報道発表資料より)