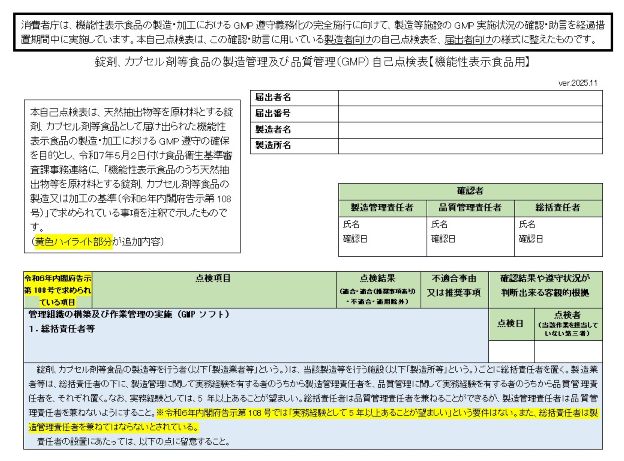
サプリGMP基準遵守の自己点検表 【機能性表示食品】消費者庁が「届出者向け版」作成
機能性表示食品のうち「天然抽出物等を原材料とする錠剤、カプセル剤等食品」(以下、サプリメント)の要件となったGMP(適正製造規範)基準に従った製造・品質管理が実施できているかどうかを、届出者自ら確認するための自己点検表を消費者庁が作成し、26日に公表した。
小林製薬「紅麹サプリ」健康被害問題を受け、機能性表示食品制度は昨年9月に改正された。これにより、機能性表示食品のサプリメントについては、法令に基づくGMP基準に従った製造管理や品質管理が実質的に義務化され、届出者には基準の遵守状況の自己点検と評価、さらにその結果を年1回、消費者庁へ報告することが義務付けられた。
GMP基準を定めた法令(内閣府告示)では、基準に従った製造等の確保は「届出者の責務」と規定されている。だが、機能性表示食品に限らずサプリメントの製造や品質の管理は、販売会社の委託を受けたOEM・ODMメーカーが行っている場合が非常に多い。同庁は、自己点検表を、販売会社を中心とする届出者が基準の遵守状況を点検・評価する際に活用してもらう考えだ。
ただし同庁は、今回公表した自己点検表は「現時点におけるもの」だと説明しており、今後、必要に応じて修正される可能性がある。
今後「指針」作成へ
機能性表示食品のサプリメントのGMP基準は昨年9月に施行。来年8月末まで経過措置期間が設けられているため、完全実施は同年9月1日となる。それに向けて同庁は今年4月、食品表示課に「GMPチーム」を新設した。
GMPチームは5月から、全国のサプリメントの製造・加工施設を直接訪れ、基準の遵守状況の確認と助言を順次進めている。同庁によると、その際に使用している自己点検表の様式を届出者向けに整えたものが、今回公表された自己点検表だ。
製造者向けの自己点検表は、サプリメントの安全性自主確保指針である通称「3.11通知」の別添2「錠剤、カプセル剤等食品の製造管理及び品質管理(GMP)に関する指針(ガイドライン)」(GMP指針)の実効性を高めるために、同通知を所管する消費者庁の食品衛生基準審査課が作成した「錠剤、カプセル剤等食品の製造管理及び品質管理(GMP)自己点検表」を土台に作成された。そもそも、機能性表示食品のサプリメントGMP基準は、GMP指針をほぼそのまま告示に引き上げるかたちで成り立っている。
機能性表示食品のサプリメントの届出者が製品の製造・品質管理に関する責務を果たせるようにするため、同庁は今後、GMPチームが進めている基準遵守状況の確認・助言などの状況を踏まえ、自己点検表を含む指針を作成する方針だ。
【石川太郎】
(冒頭の画像:機能性表示食品のサプリGMP自己点検表の冒頭ページ)
関連資料
:「天然抽出物等を原材料とする錠剤、カプセル剤等食品として届け出られた機能性表示食品の製造又は加工の基準に準拠した体制に係る自己点検表について」(消費者庁ウェブサイトへ)
:自己点検表(同上)※以下のページ下部にある「その他届出関連資料」から、Word形式でダウンロード可能
関連記事
:消費者庁食品表示課保健表示室に聞く 改正・機能性表示食品制度の運用実態と課題(後編)
:消費者庁、GMP実施状況確認へ 機能性表示食品のサプリ製造工場対象に立ち入り、事前に「自己点検」要請も
:3.11通知GMP指針に自己点検表 消費者庁が作成、サプリの製造・品質管理に活用求める
:改正・機能性表示食品制度の告示案 「自己点検等報告」にみる原材料の品質確保策