届出撤回の理由、関与成分の含有量 【機能性表示食品届出DB更新】届出者が明かす、表示を「下回っていた」
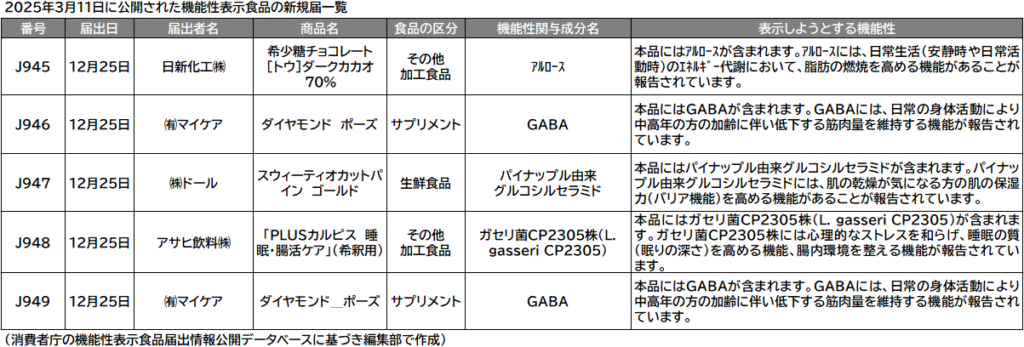
機能性表示食品の届出情報データベースが11日、更新された。新たに公開された新規届出は5件(サプリメント2件、サプリ以外の加工食品2件、生鮮食品1件)で、新規の機能性関与成分等はなかった。一方、撤回届出は前回6日の更新から14件増えた。機能性関与成分の含有量が届け出た表示値を下回っていたことを理由にした撤回があった。
「販売されている商品中の機能性関与成分の含有量が届け出られた含有量を下回っておりました。適切な改善措置や再発防止の社内体制が整えることに注力し、現時点での機能性表示食品の継続販売は行わないことといたします」(原文ママ)
こうした理由で、イチョウ葉由来フラボノイド配糖体および同由来テルペンラクトンを機能性関与成分として配合したサプリメント(ハードカプセル)の届出を取り下げたのは、㈱田尻300年製薬(熊本県玉名市)。消費者庁が定期的に行っている買上調査で、機能性関与成分の含有量が届出を下回っていたことが判明したとみられる。
撤回は、今月4日付け。含有量が届出を下回っていた機能性関与成分はテルペンラクトンで、1日摂取目安量2粒当たり4.8mg含有する旨を届け出ていたものの、少なくとも昨年6月に製造された製品(製造数量50袋、賞味期限27年6月26日)は、これを満たしていなかった。同社は取材に、「だいぶ少なかったと聞いている」と答えた。フラボノイド配糖体については届出のとおり(2粒当たり19.2mg)だったと伝えられているという。
製造は、玉名市に置く自社工場で行っていた。機能性関与成分の含有量が少なかったことを同社が認識したのは、熊本県と管轄の有明保健所からの指摘による。先月26日までに指摘され、対応を求められ、自主的に届出を撤回。現在までに回収などを済ませた。機能性関与成分の含有量が少なかったことの他に、製品の内容量が届け出ていた40.92g(660mg×62粒)に満たなかったこと(粒数自体は届出のとおりだった)、賞味期限3年の設定根拠が不明瞭であったことも併せて指摘されたという。
同社は先月26日付で、自社ウェブサイトに「製品不良に関するお詫びとお知らせ」を掲載。保健所から指摘された事実を公表し、「社内の確認体制及び品質管理体制を見直すと共に、関連法規の遵守を徹底してまいります」とした。
同社は一般用医薬品の製造も行っている。その中で、サプリメントの製造・品質管理に関するGMP第三者認証は取得していなかった。機能性関与成分の含有量が定めた量よりも少なかったなどした製品不良の原因は「現在調査中」。機能性表示食品は他にも数品目を届け出ているが、すべての届出を近く撤回し、サプリメントの製造・品質管理体制を見直す。その上で、改めて届出を行いたいという。
【石川太郎】
関連資料:田尻300年製薬「製品不良に関するお詫びとお知らせ」(同社ウェブサイトへ)
25年3月のDB更新:【5日】MSM、膝関節ケアの関与成分に 新たな届出者に東和薬品ヘルスケア
:【6日】ツボクサエキス、機能性表示に対応 アシアチン酸等を機能性関与成分に






















