小林製薬、紅麹原料で報告漏れ 52社のうち1社、173社のうち4社が該当
小林製薬㈱(大阪市中央区)はきのう26日、厚生労働省に対して3月29日と4月4日に行った報告に不備があったことをホームページ上で発表、謝罪した。
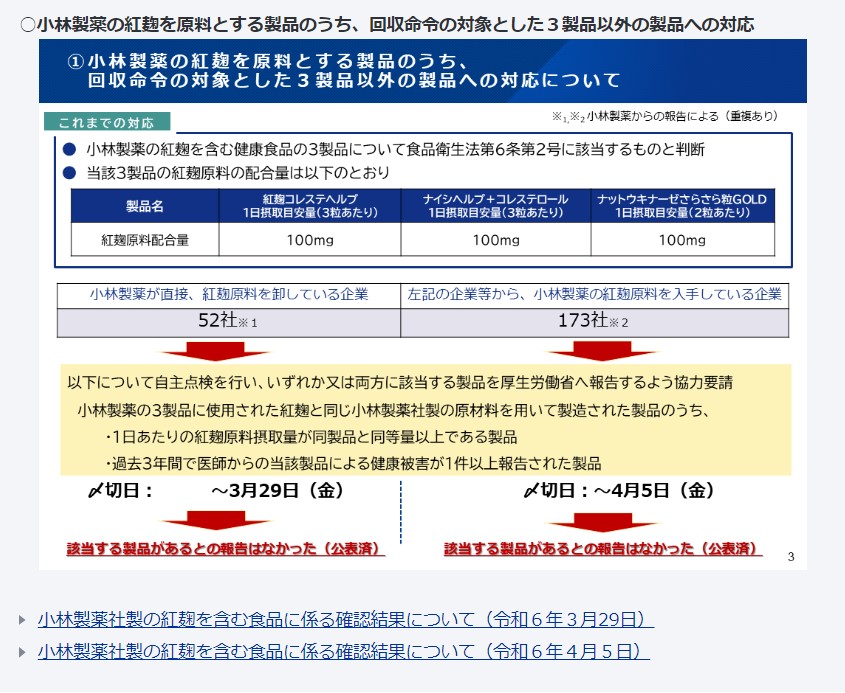
厚生労働省は紅麹問題が発覚した後、同社の紅麹含有サプリ3製品を食品衛生法第6条第2号(有害物質を含む食品)に該当すると判断し、大阪市を通じて自主回収を命じた。
OEM製品で「100㎎/日」配合が判明
同時に厚労省は、小林製薬のグループ会社が直接、同社製紅麹原材料を卸していた52社と、52社から紅麹原材料を入手していた173社に対して、①小林製薬の3製品に使用された紅麹と同じ同社製の原材料を用いて製造、かつ、1製品に100㎎以上の紅麹を1日当たりに摂取する製品、②過去3年間で医師から健康被害が1件以上報告された製品———の有無を調べて報告するよう求めていた。
52社に対する自主点検の締切は3月29日、173社に対しては4月5日を報告の最終期限と定めたが、当時、共に該当する製品は1件もなかった。
厚労省によれば、自主点検対象の製造業者の製品に関する自主回収届出を受理した地方自治体からの照会があり、同省が小林製薬に確認を求めたところ、同社からの報告に不備があったことが判明したという(厚労省発表)。
小林製薬は昨日、52社のうち1社、173社のうち4社から報告された製品について、①の要件を満たす製品があるとの報告を受けていたにもかかわらず、厚労省に対する報告が漏れていたことを明らかにした。報告が遅れた理由について、(小林製薬が直接販売することのない)OEM製品については販売会社自らに報告義務があるものと判断したという。またしても、身勝手な判断基準に基づいた報告漏れとなってしまった。
同社は厚労省の求めに従い、遅くとも31日までに正確な報告ができるように精査中だという。
自見大臣が「調査報告書」の虚偽を指摘
消費者・食品安全担当大臣の自見はなこ氏はきのう26日の記者会見で、23日に小林製薬が公表した「調査報告書」についてコメント。「一般的な衛生管理に基づく基本的な製造の管理がなされていなかったということを改めて認識した」と憤りを見せた。さらに同社が健康被害の行政への報告について「因果関係が明確な場合に限る」との身勝手な解釈基準を採用していたために報告が2カ月遅れたことに対して遺憾の意を述べた。
さらに、調査報告書43ページ「3.10.1 行政報告」における記載について指摘した。「国内品質保証監査グループの機能性表示食品の担当者は、3月 21日(木)夕方、消費者庁へ電話連絡を行い健康被害報告を行いたい旨申し入れ、同庁との日程調整の結果、面談は 同 月 22日(金) に設定された」とする部分について、自見大臣は、そのような事実はないと否定。
「消費者庁としては3月21日同日中の面会を大変しっかりと求めさせていただいたが、小林製薬側からご自分の会社の準備があるため、3月22日15時より早い時間で対応することは困難である、難しいという旨の回答であったことから、やむを得ず翌日22日の15時からのオンラインで面談をすることとなったもの」とし記載自体が事実と異なるものだと重ねて否定した。小林製薬にも強く申し入れを行っているという。
【田代 宏】






















