改正17年通知の施行、来年1月か 指定成分GMPに寄せた改正案、厚労省が意見募集を開始
厚生労働省はきょう(21日)、健康食品のうちサプリメント形状(錠剤、カプセル剤、粉末剤、液剤など)の製造・品質管理に関する考え方を示したガイドライン案を公表し、意見募集を始めた。同案は、厚労省が2005年に作成した、事業者に適正製造規範(GMP)へ自主的に取り組むことを求めるいわゆる「平成17年通知」の改正案。来月20日まで意見募集を行い、来年1月下旬の予定で施行するという。施行にともない同通知は廃止される。
平成17年通知の正式名称は、「『錠剤、カプセル状等食品の適正な製造に係る基本的考え方について』及び『錠剤、カプセル状等食品の原材料の安全性に関する自主点検ガイドライン』」。
これを廃止し、「『錠剤、カプセル剤等食品の原材料の安全性に関する自主点検及び製品設計に関する指針(ガイドライン)』及び『錠剤、カプセル剤等食品の製造管理及び品質管理(GMP)に関する指針(ガイドライン)』」に改める。
健康食品のうち、2018年施行の改正食品衛生法に基づき制度化された指定成分等含有食品には、GMPに基づく製造・品質管理を義務付けている。一方、厚労省は、それ以外の健康食品についても「錠剤、カプセル状等の成分が濃縮された形状の食品に関しては、一定の製造・品質管理が必要」、「各々の原材料の安全性を適切に評価し、一定の品質の製品を製造する重要性がさらに増している」などと指摘。そのため、平成17年通知を廃止し、指定成分等含有食品に義務付けているGMPの内容を踏まえ、「製造・品質管理の考えた方を含めたガイドラインを新たに示し明確化する」と説明している。
厚労省では、ガイドライン案の概要について以下のとおり説明している。
- ガイドライン全体の構成について、原材料の安全性確保及び適切な製品設計を行ったうえで、GMPに基づく製造が行われることが重要であること等を踏まえたものとした。(別紙の別添1及び別添2)
- 本ガイドライン(案)における対象の範囲、定義について明確化し、ほか用語の整理等を行った。
- 別添1に関して、原材料の安全性に関する自主点検の考え方について明確化し、製品設計における留意事項についての記載を追加した。また、原材料の安全性に関する自主点検フローチャートについて、全体の見直しを行った。
- 別添2に関して、指定成分GMPと整合を図る形でより具体的な記載とし、全体を明確化した。また、GMPに加え食品衛生法に基づく衛生管理を行うよう留意することを追記した。
【石川太郎】
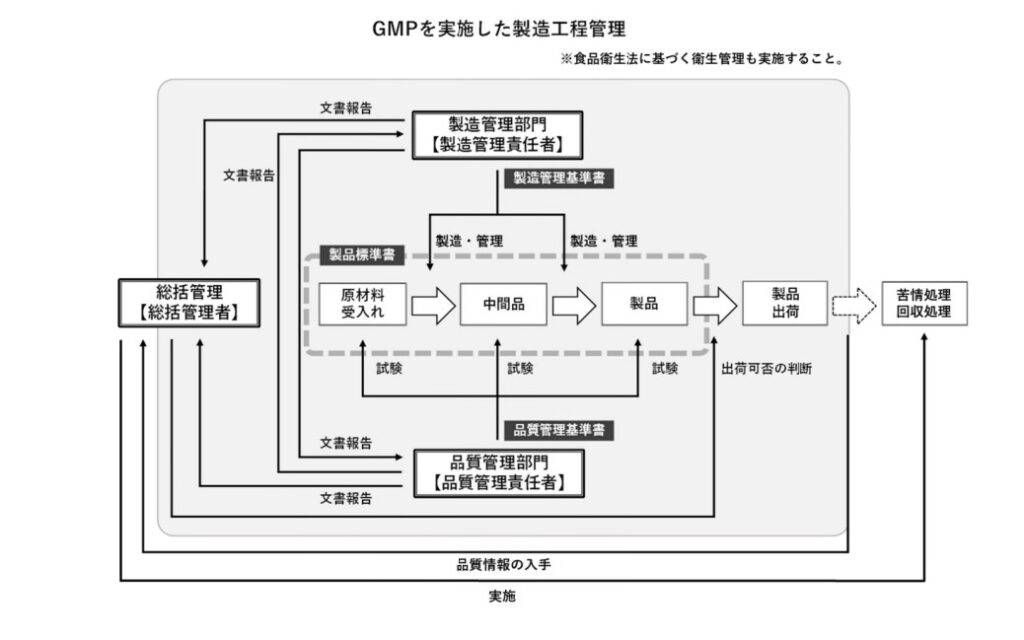
(下の画像:GMPを実施した製造工程管理のフロー図。ガイドライン案から)
関連資料(パブリックコメントのサイトへ)
:改正案の概要
:各ガイドライン案(別添1、別添2)
関連記事
:17年通知改正へ、厚労省が改正案 指定成分GMPとの整合図る
:14年通知も正へ、厚労省、健康被害疑い情報の収集強化




















